Michael付加反応(マイケル付加反応)は、有機化学で広く知られる反応の一つで、エノラートなどの求核種がα,β-不飽和カルボニル化合物(Michaelアクセプター)に付加する反応です。
本記事では、Michael付加反応の仕組みや応用例、そして条件について詳しく解説します。
Michael付加反応とは?
Michael付加反応は以下のような一般式で表されます:
\(
\text{Nu}^- + \text{R}_1\text{-CH=CH-C=O-R}_2 \rightarrow \text{R}_1\text{-C(Nu)-CH}_2\text{-C=O-R}_2
\)
ここで:
- Nu⁻:求核剤(エノラート、アミン、チオールなど)
- R₁-CH=CH-C=O-R₂:α,β-不飽和カルボニル化合物(Michaelアクセプター)
この反応では、求核剤がアルケン部分(C=C)に付加し、β位に結合します。このため、「1,4-付加反応」とも呼ばれます。
反応機構
ステップで見ると
多くの場合、求核剤(Nu⁻)は塩基によるプロトンの除去などで生成されます。例えば、カルボニル化合物からエノラートが形成されます:
\(
\text{R-CH}_2\text{-C=O} + \text{Base} \rightarrow \text{R-CH=CH-C(O)}^-
\)
求核剤がα,β-不飽和カルボニル化合物のβ位を攻撃し、炭素−炭素結合を形成します。
付加後に生成されるエノラート中間体は、プロトン化または異性化を経て安定な付加生成物を得ます。
具体的に図で書くと
具体的に図で書くとこんな感じです。
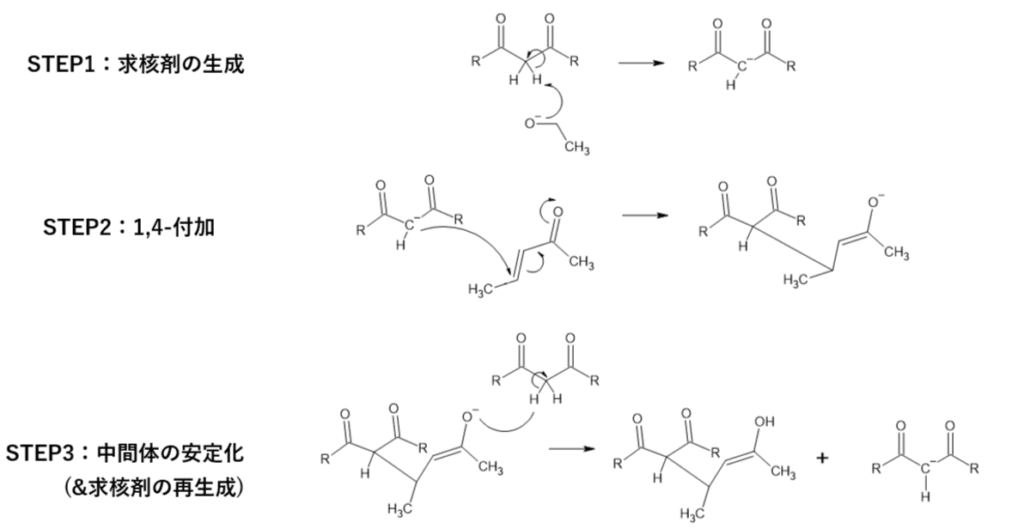
反応の特徴
1. 反応性
Michael付加反応は、特に以下の条件下で進行します:
- 求核剤:エノラート、アミン、シアン化物イオン、またはチオールなど。
- アクセプター:α,β-不飽和カルボニル化合物(例:エノン、エステル、ニトリル)。
2. 1,4-付加と1,2-付加の競合
求核剤の性質や反応条件によっては、1,2-付加(カルボニル炭素への付加)が起こる場合もあります。
しかし、比較的安定なアニオン性求核剤と反応する場合には、比較的高エネルギーのアルコキシドが生成するため、可逆的です。
一方で1,4付加は共役安定化されたエノラートイオンを生成するので熱力学的に有利というわけです!
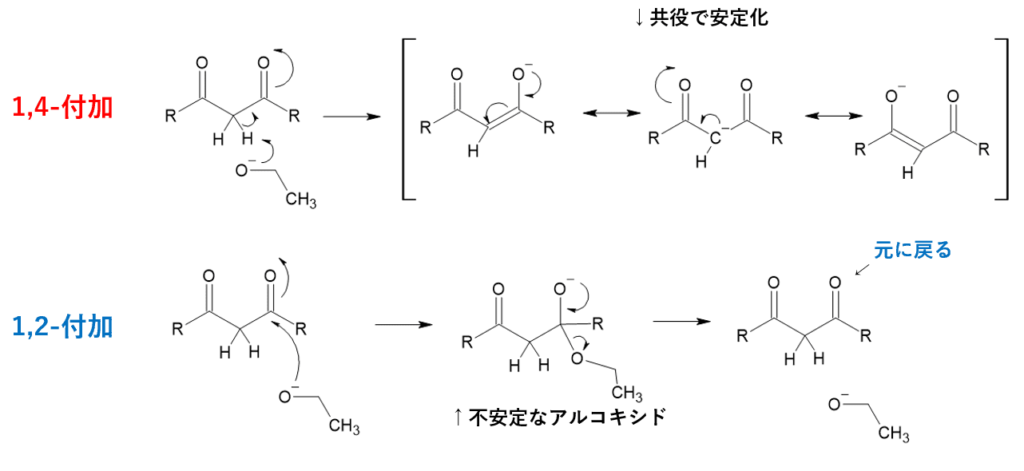
3. 実験条件について
① 塩基性条件
エノラートを生成するため、弱塩基(例:NaOH、K₂CO₃)や強塩基(例:LDA)が使用されます。
② 酸性条件
チオールやアミンのような求核剤を使う場合、酸性条件下でもMichael付加が進行します。
③ 溶媒
溶媒には極性溶媒(DMF、DMSOなど)が用いられます。特に溶媒の選択は、反応速度と生成物の選択性に影響を与えます。
練習問題
練習問題も作ったので良ければ解いてみて下さい。
プロパン二酸ジエチルと3-ブテン-2-オンのMichael付加の反応機構を電子の矢印を用いて書け。
ただし、触媒として、ナトリウムエトキシドを少量用いている。
解答
解答は以下の通りです!
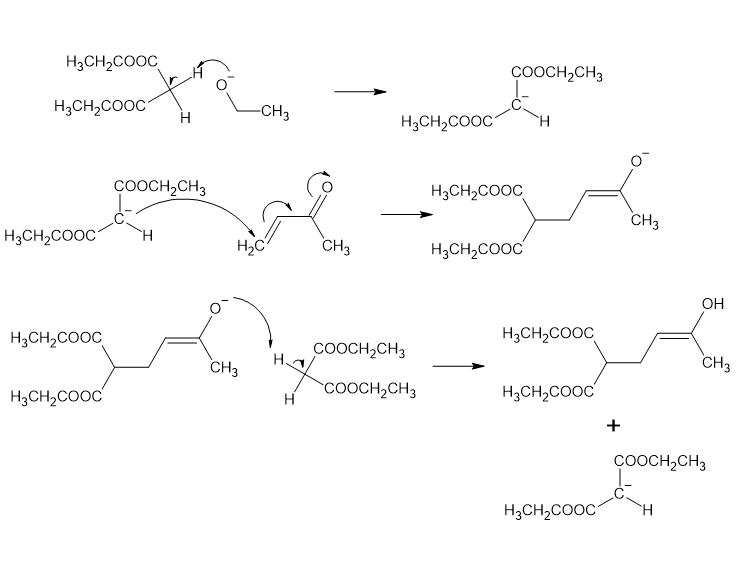
求核剤の生成→1, 4付加→エノラートイオンのプロトン化(および求核剤の再生成)の順に進行していますね!
まとめ
Michael付加反応は、有機化学において重要なC-C結合形成反応です。
その反応性と選択性により、合成化学や材料化学、生化学など幅広い分野で応用されています。本記事で紹介した反応機構や条件を理解することで、さまざまな応用分野でMichael付加反応を活用できるかもしれません!

コメント