有機化学を学ぶ大学生にとって、「反応機構」の理解は最大の壁の一つです。教科書に書かれている複雑な生成物を見て、「なぜこの結合が切れて、ここに新しい結合ができるの?」と頭を抱えた経験はあるでしょう。
その「なぜ」を説明する言語こそが、「曲がった矢印」です。
曲がった矢印は、単なる飾りではありません。化学反応における電子の動きを可視化するツールです。
この矢印の書き方をマスターすれば、未知の反応に出会っても、ある程度メカニズムを推測できるようになります。丸暗記の化学から卒業するための必須スキルです。
この記事では、化学系大学生向けに、反応機構図における「曲がった矢印」の正しい書き方、ルール、そして典型的なパターンを徹底解説します。
大原則:矢印は「電子対」の動きを表す
最も重要で、絶対に忘れてはいけない大原則があります。
曲がった矢印は、常に「電子対(2個の電子)」の移動方向を表す。 原子核(原子そのもの)や、正電荷(プラス)の動きを表すものではない。
有機反応の多くは、電子が豊富な場所から、電子が不足している場所へ移動することで起こります。この「電子の流れ」を追うのが矢印の役割です。
- 通常の曲がった矢印(二重の矢尻): 電子対(2電子)の移動を表します。イオン反応のほとんどはこれです。
- (参考)片方の矢尻(釣り針状): ラジカル反応における1電子の移動を表します。今回は扱いません。
矢印の「始点」と「終点」
矢印を正しく書くためには、「どこから始まり(始点)」、「どこへ向かうか(終点)」を明確にする必要があります。
始点:電子が豊富な場所
矢印の尻尾は、必ず電子がある場所からスタートします。具体的には以下の3つです。
- 非共有電子対:
- 最も一般的な始点です。N, O, S, ハロゲンなどが持つ孤立電子対です。
- (例:アンモニアのNの孤立電子対、水酸化物イオンのOの孤立電子対)
- π結合(パイ結合):
- 二重結合や三重結合にある、反応性の高い電子対です。
- (例:アルケンのC=C二重結合)
- σ結合(シグマ結合):
- 単結合の電子対が移動することもあります。脱離反応や転位反応で見られます。
- (例:C-H結合が切れてH⁺が取れる時、C-L結合が切れて脱離基Lが抜ける時)
【重要キーワード】 これら「電子対を与える能力がある種」を求核剤またはルイス塩基と呼びます。
終点:電子を受け入れる場所
矢印の先は、電子を受け入れることができる場所に向かいます。
- 電気陰性度の高い原子(δ-):
- 新しい結合を作るために、その原子に向かって矢印を引きます。ただし、その原子がすでにオクテットを満たしている場合、同時に別の結合を切断して電子を押し出す必要があります(後述)。
- 正電荷を持つ原子(カチオン)または部分正電荷(δ+)を持つ原子:
- 電子が不足している場所は、喜んで電子を受け入れます。
- (例:カルボカチオンの空のp軌道、カルボニル基の炭素(C=OのCはδ+))
- 原子と原子の間の空間(新しい結合の形成):
- 新しいπ結合ができる時など、原子間結合の上に矢印の先を置くことがあります。
【重要キーワード】 これら「電子対を受け取る能力がある種」を求電子剤またはルイス酸と呼びます。
習得すべき4つの基本パターン
有機反応機構は複雑に見えますが、実は基本的な電子移動パターンの組み合わせで成り立っています。まずはこの4つを完璧に理解しましょう。
パターンA:求核攻撃(Nucleophilic Attack)
電子豊富な種(求核剤)が、電子不足な種(求電子剤)を攻撃して新しい結合を作るパターンです。
[例:Brイオンによるカルボカチオンへの攻撃]
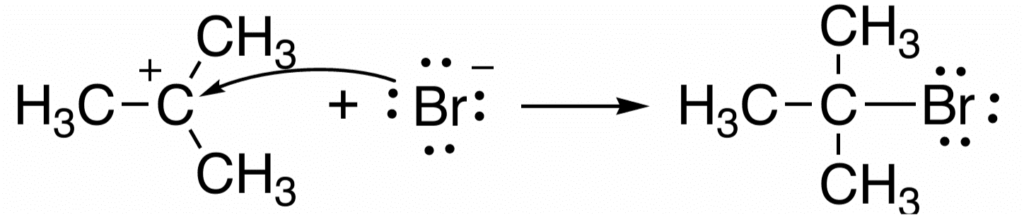
新たに生成した結合の電子は、もともとBrが持っていた非共有電子対から来ています。
パターンB:脱離基の脱離(Loss of a Leaving Group)
単結合(σ結合)の電子対を持って、原子団が分子から離れるパターンです。さっきと逆ですね。
[例:tert-ブチルブロミドからの臭化物イオンの脱離]
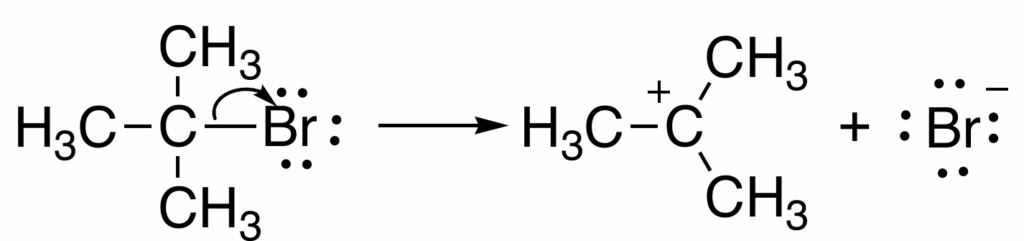
C-Br結合の電子対がBrのものになり、Br⁻として脱離します。残されたCはプラスになります。
パターンC:プロトン移動(Proton Transfer)
酸塩基反応のことです。
「塩基がH⁺を奪う」反応ですが、H⁺が動くのではなく、塩基の電子対がHを取りに行くように描くのが鉄則です。
これはパターンAとBの組み合わせで起こることが多いです。
[例:水酸化イオンと塩化水素の反応]
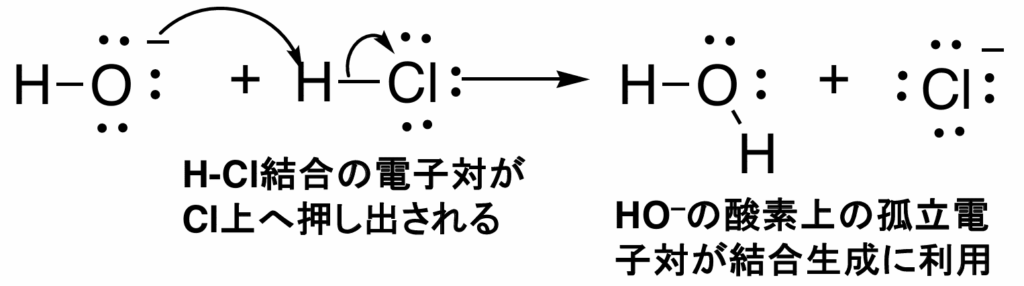
- OH–の非共有電子対(始点)から、HClのH(終点)へ矢印を引く(Hへの攻撃)。
- 同時に、H-Cl結合(始点)からCl(終点)へ矢印を引く(Clの脱離)。 ※Hは結合を1本しか持てないため、新しい結合ができると同時に、古い結合を切る必要があります。
パターンD:転位(Rearrangement)※ややレア
不安定な中間体(カルボカチオンなど)が、より安定な構造へ変化する際に起こります。隣の炭素からHやメチル基が、電子対ごと移動します。
[例:カルボカチオンのヒドリドシフト]
隣接するC-H結合(始点)が、電子対ごとカチオン中心の空軌道(終点)へ移動します。
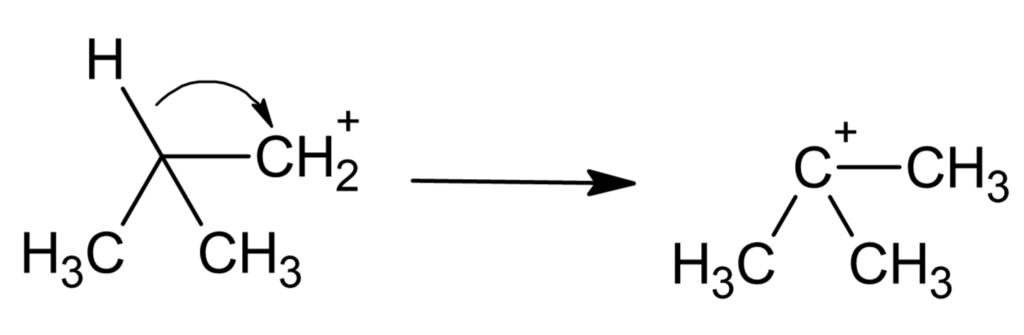
ちなみにカルボカチオンの安定度は、超共役の効果により第一級<第二級<第三級カルボカチオンの順番なので、この反応はいたって自然ですね!

絶対に守るべきルールと注意点
矢印を書く際に、以下のルールを破ると化学的にありえない構造になってしまいます。常に意識しましょう!
ルール1:オクテット則を決して破らない(特に第2周期元素)
C, N, O, F などの第2周期元素は、価電子を8個(結合4本分)までしか持てません。 炭素に結合の手を5本生やしてはいけません。
- すでに結合が4本ある(あるいは二重結合などでオクテットを満たしている)原子に対して求核攻撃をする場合は、必ず同時に別の結合を切断して、電子を押し出す矢印(脱離の矢印)を書く必要があります(パターンCの例を参照)。
ルール2:形式電荷の変化を正しく追う
電子対が移動すると、原子の形式電荷が変わります。これを間違えると反応機構が破綻します!
- 電子対を受け取った原子:形式電荷は「-1」方向に変化します。
- 中性 → 負電荷 (0 → -1)
- 正電荷 → 中性 (+1 → 0)
- 電子対を供与した(失った)原子:形式電荷は「+1」方向に変化します。
- 中性 → 正電荷 (0 → +1)
- 負電荷 → 中性 (-1 → 0)
例)中性のNH₃が非共有電子対を使ってH⁺と結合すると、Nは電子を供与した形になるので、NH₄⁺(正電荷)になります。
注意点:逆向きの矢印を書かない
初心者がやりがちなミスです。
×「H⁺が、電子豊富な二重結合に近づいていく」 〇「二重結合のπ電子が、H⁺を捕まえにいく」
常に主語は「電子」です。プラスの電荷から矢印をスタートさせてはいけません!
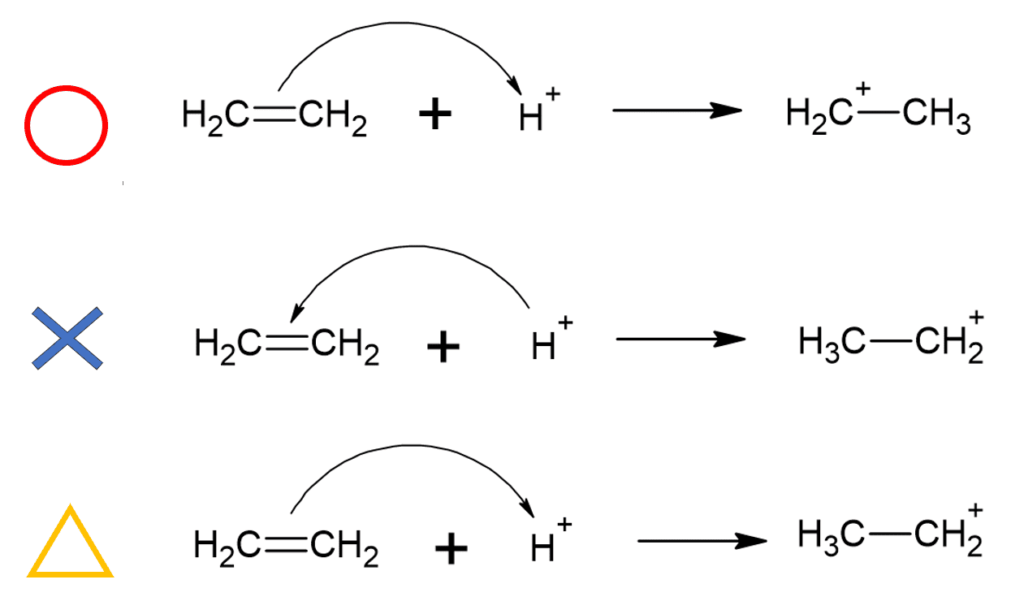
補足
これは補足ですが、「矢印のえがく円の外側」にある原子の電子対が移動します。
上の図にある通り、△で示した反応機構は左側のC原子上の電子対が使われているのに最終的に右側のC原子がC+になっているので、少し気持ちの悪い反応機構になっています。
どれくらい気持ち悪いかというと、数学の割り算で6÷2=3・・・0と書くぐらいです。
もし右側のC原子をC+にしたいのなら、以下のように書く必要があります。
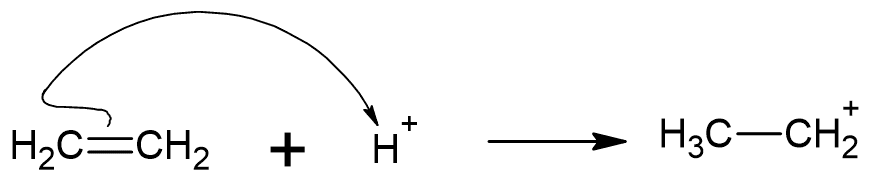
練習問題
少しですが、練習問題を用意しました。時間があれば解いてみて下さい!
練習問題①
\(\ce{CH2=CH2 + H+ -> CH2+CH3}\)
この反応機構を電子の巻き矢印を用いて書け。
答え

二重結合から矢印がスタートするのがポイントです!!!
練習問題②
\(\ce{NH3 + H2O -> NH4+ + OH-}\)
この反応機構を電子の巻き矢印を用いて書け。
答え

今回は窒素原子の非共有電子対から電子がスタートします!
まとめ
反応機構の矢印は、有機化学における「言語」です。最初はぎこちなくても、自分で手を動かして書いていくうちに、電子の流れが自然に見えるようになります。
- 矢印は「電子対」の動き!
- 始点は「非共有電子対、π結合、σ結合」!
- 終点は「δ+の原子、カチオン、新しい結合位置」!
- オクテット則と形式電荷に注意!
教科書を読む時も、ただ目で追うだけでなく、「なぜここに矢印が引かれているのか?(どの電子が、どこに惹かれているのか?)」を常に考える習慣をつけましょう。それが有機化学マスターへの近道です。

コメント