お酢に含まれる酢酸や、柑橘類に含まれるクエン酸。これらはすべて「カルボン酸」と呼ばれる有機化合物の仲間です。
名前の通り、これらは「酸性」で、水溶液中で電離して水素イオン(H⁺)を放出します。
でも、ちょっと不思議に思いませんか?
同じように「-OH(ヒドロキシ基)」を持つアルコール(エタノールなど)は中性なのに、なぜカルボン酸(-COOH)の「-OH」からはH⁺が外れやすいのでしょうか?
その理由は、H⁺が外れた後の「アニオン(陰イオン)」の姿に隠されています。今回は、有機化学の超重要概念である「共鳴」と「誘起効果」を使って、その謎を解き明かしましょう!
大原則:酸の強さは「H⁺を出した後の安定性」で決まる!
酸性の理由を考える前に、絶対に押さえておきたい大原則があります。
物質がH⁺を放出して酸性を示す反応は、平衡反応です。
$$R-COOH \rightleftharpoons R-COO^- + H^+$$
(カルボン酸 $\rightleftharpoons$ カルボキシラートイオン + 水素イオン)
この反応が右に進みやすい(=H⁺を出しやすい=強い酸である)かどうかは、生成物である「カルボキシラートイオン(R-COO⁻)」がいかに安定かにかかっています。
もし、H⁺を出した後のイオンが不安定なら、すぐにH⁺と再結合して元に戻ってしまいます。逆に、H⁺を出した後のイオンがとても安定なら、喜んでH⁺を放出した状態を保とうとします。
つまり、「カルボン酸が酸性を示すのは、カルボキシラートイオン(R-COO⁻)が非常に安定だから」と言い換えることができます。
では、なぜそんなに安定なのでしょうか? 2つの理由があります。
理由1:共鳴による安定化(電子の分散)
最大の理由は「共鳴(きょうめい)」です。
カルボキシラートイオン(R-COO⁻)の構造を見てみましょう。一つの酸素原子にマイナスの電荷(負電荷)が集中しているように見えます。
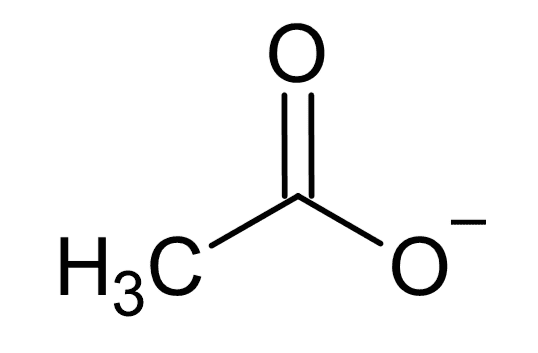
しかし、実際にはこの二重結合の位置と、負電荷の位置は固定されていません。隣り合う酸素原子の間で、π電子(パイ電子)が行ったり来たりすることができます。
これを「共鳴構造式」で書くと、以下のようになります。
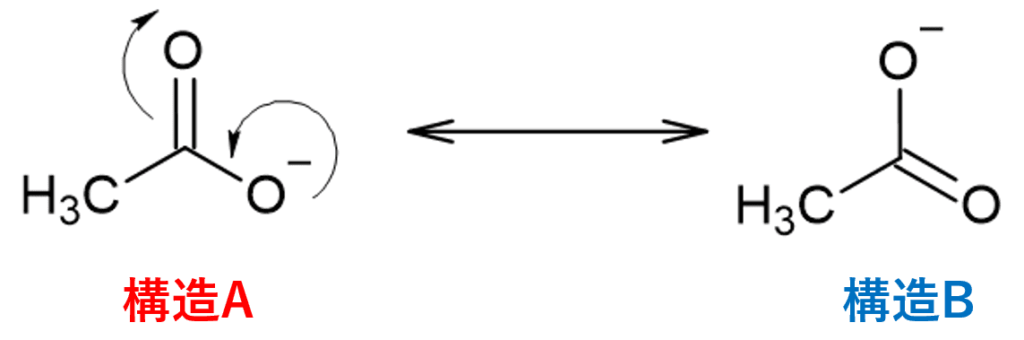
構造Aと構造Bを行ったり来たりしている(共鳴している)ことで、マイナスの電荷は一つの酸素原子に集中せず、二つの酸素原子全体に薄く広がって(非局在化して)存在しています。
重たい荷物(負電荷)を一人(一つの酸素原子)で持つより、二人(二つの酸素原子)で分担して持つ方が楽(安定)ですよね。
この「電子が広い範囲に分散して安定化する」現象が共鳴であり、これがカルボキシラートイオンが安定である最大の理由です。
理由2:誘起効果(電気陰性度による引き寄せ)
もう一つの理由が「誘起効果(ゆうきこうか)」です。これは原子の電気陰性度の違いによって、結合の電子が引っ張られる効果のことです。
カルボン酸の構造(R-COOH)には、カルボニル基(C=O)が含まれています。
酸素(O)は炭素(C)よりも電気陰性度が非常に高いため、C=O結合の電子は酸素側に強く引っ張られています。
$$R – \overset{\delta+}{C}(=\overset{\delta-}{O}) – O – H$$
(炭素Cはわずかにプラス、酸素Oはわずかにマイナスを帯びます)
すると、その影響は隣のC-O結合、さらにその隣のO-H結合にも伝わります。
- カルボニル基の炭素(C)が電子不足(δ+)になる。
- その炭素が、隣のヒドロキシ基の酸素(O)から電子を引っ張る。
- 電子を引っ張られた酸素は、さらに隣の水素(H)との結合電子(O-H結合の電子)を自分の方へ強く引き寄せる。
結果として、O-H結合の電子対は酸素側に大きく偏り、水素原子はH⁺として非常に外れやすい状態になります。
また、H⁺が外れた後にできる負電荷も、カルボニル基の強力な電子求引性(電子を引っ張る性質)によって、分子全体に分散されるのを助け、さらに安定化します。
【比較】なぜアルコールは中性なのか?
比較対象として、同じ「-OH」を持つアルコール(R-OH)を見てみましょう。
アルコールがH⁺を出した後のイオンを「アルコキシドイオン(R-O⁻)」と呼びます。
$$R-OH \rightleftharpoons R-O^- + H^+$$
このアルコキシドイオン(R-O⁻)には、カルボキシラートイオンのような安定化の仕組みがありません。
- 共鳴できない: 隣に二重結合がないため、負電荷を分散できません。一つの酸素原子に負電荷が集中してしまいます(不安定)。
- 強い誘起効果がない: カルボニル基(C=O)のような強力に電子を引っ張るグループがいません。
そのため、アルコキシドイオンは不安定であり、すぐにH⁺と戻ってしまいます。だからアルコールはH⁺をほとんど放出せず、中性(ごくごく弱い酸性)なのです。
まとめ
カルボン酸が酸性を示す理由は、H⁺を放出した後の「カルボキシラートイオン」が非常に安定だからです。その安定化には、以下の2つの効果が働いています。
- 共鳴効果: 負電荷が2つの酸素原子上に分散される。
- 誘起効果: カルボニル基(C=O)の高い電気陰性度により、O-H結合の分極が進み、アニオンの負電荷も安定化される。
この二つの合わせ技によって、カルボン酸は有機化合物の中では比較的強い「酸」としての性質を持つのです。

コメント