有機化学を学んでいると、カルボカチオンやラジカルの安定性を議論する場面で必ず登場する言葉があります。それが「超共役(Hyperconjugation)」です。
「共役」は二重結合と単結合が交互に並ぶやつでしょ?じゃあ「超」共役って何?
教科書の説明を読んでも、いまいちイメージが掴みにくい…と感じている人も多いのではないでしょうか。
この記事では、そんな「超共役」の正体について、図を用いながら直感的に理解できるように徹底解説します。これを読めば、有機反応の「なぜそうなるのか?」が、より深く理解できるようになるはずです。
超共役を一言でいうと?
まず結論から言いましょう。超共役とは、
「σ結合(シグマ結合)の電子が、隣にある空っぽの軌道(または半占有軌道)に染み出して、分子全体を安定化させる効果」
のことです。
通常の「共役」は、π電子(パイ電子)がp軌道を通じて非局在化する現象でした。
それに対し「超共役」は、本来は強固で動かないはずのσ電子が非局在化に参加するという、まさに「超」法規的な現象なのです。
【核心】なぜ安定化するのか?(軌道のイメージ)
超共役の理解には、軌道のイメージが不可欠です。ここでは「エチルラジカル」を例に見てみましょう。
ここでは「ラジカル」を例に出しますが、「カチオン(C+)」であっても超共役の原理は同じです!
2-1. ラジカルの悩み
ラジカルの炭素は、電子が1つ足らない状態です。そして、そこには電子が1つしか入っていないp軌道があります。この軌道は非常に不安定で、「電子が欲しい!」と常に渇望しています。

2-2. 隣人の助け(σ結合からの電子の染み出し)
ここで、隣の炭素(メチル基)を見てみましょう。ここには、C-H間のσ結合があります。σ結合には電子対(2つの電子)が詰まっています。
もし、このC-Hσ結合の軌道が、隣のp軌道と同じ向きになると、何が起こるでしょうか?
σ軌道に入っている電子雲の一部が、隣のp軌道の方へ少しだけ「染み出す(重なり合う)」ことができます。


これが超共役の正体です。
- 電子不足のp軌道は、隣から少し電子を分けてもらえて、渇きが癒やされます(安定化)。
- 電子を供与したC-H結合は、電子密度が少し減って結合が弱くなりますが、分子全体としては、電子が狭いσ結合に閉じ込められているより、広い範囲(p軌道まで含めた範囲)に広がった方が、エネルギー的に安定になります。
【ポイント】超共役は、C-H結合が完全に切れてH⁺が外れるわけではありません。「結合は保ったまま、電子だけ少し貸してあげる」という絶妙な助け合いなのです。
超共役の効果が現れる場面
超共役は、電子不足な中心(空軌道や半占有軌道を持つ原子)の隣に、電子供与性のσ結合(主にC-HやC-C結合)がある場合に働きます。
① ラジカルの安定化
ラジカルは電子不足でものすごく不安定な状態です。ラジカルの炭素には電子が1つだけ入ったp軌道があります。
この軌道に対して、隣のC-Hσ結合から電子が染み出すことで安定化が起こります。
ここで安定性の順序の話ですが、ラジカルの炭素に結合しているアルキル基(メチル基など)の数が多いほど、超共役の回数が増え、より安定になります。
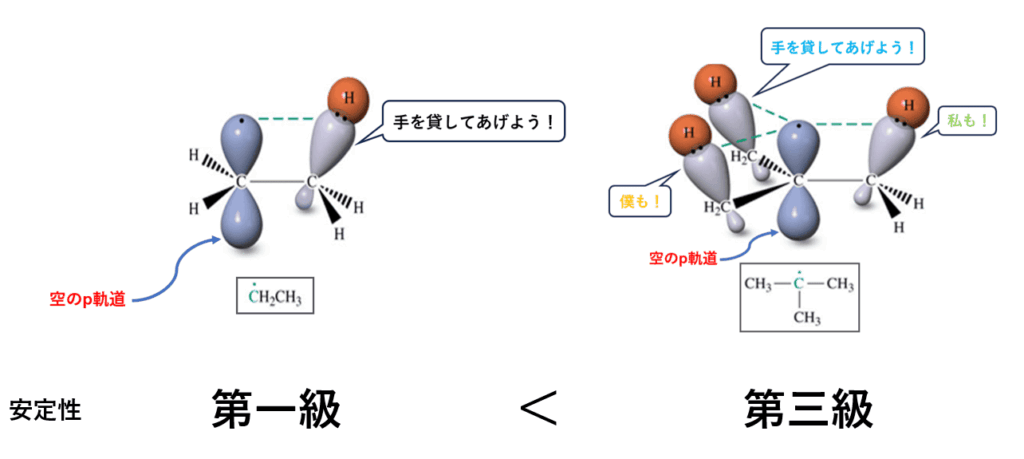
ラジカルの安定性の順序:
$$\text{第3級ラジカル} > \text{第2級ラジカル} > \text{第1級ラジカル} > \text{メチルラジカル}$$
② カルボカチオンの安定化
カルボカチオンの炭素に結合しているアルキル基(メチル基など)の数が多いほど、超共役の回数が増え、より安定になります。
カルボカチオンの安定性の順序:
$$\text{第3級} (R_3C^+) > \text{第2級} (R_2CH^+) > \text{第1級} (RCH_2^+) > \text{メチル} (CH_3^+)$$
- 第3級カルボカチオン(例:tert-ブチルカチオン):空のp軌道の周りに、C-H結合を持つメチル基が3つもあります。それぞれのメチル基から超共役による電子の援助を受けられるため、非常に安定です(合計9本のC-H結合が関与可能)。
- メチルカチオン:隣にC-H結合が全くないので、超共役による安定化はゼロです。最も不安定です。
この安定性の序列は、SN1反応やE1反応の進みやすさ、マルコフニコフ則などを理解する基礎となります。
③ アルケンの安定化(ザイツェフ則)
アルケン(C=C二重結合)の安定性も超共役で説明できます。
二重結合の炭素に結合しているアルキル基が多いほど、そのアルケンは安定になります(ザイツェフ則)。
これは、アルキル基のC-Hσ結合が、二重結合のπ*反結合性軌道(パイ・スター軌道)という空の軌道と相互作用して、安定化するためだと説明されています(少し高度な解釈です)。
$$R_2C=CR_2 > R_2C=CHR > RCH=CHR > RCH=CH_2 > CH_2=CH_2$$
置換基が多いほど、超共役のチャンスが増えるため安定です。
まとめ:超共役は「隣からの電子のおすそ分け」
いかがでしたでしょうか。難しく感じる「超共役」も、イメージさえ掴めばシンプルです。
- 何が?: 隣の炭素のσ結合(主にC-H)の電子が。
- どこへ?: 電子不足な原子の空軌道(p軌道など)へ。
- どうなる?: 電子が染み出して広がり、分子全体が安定化する。
この「隣からの電子のおすそ分け」効果こそが、有機化学反応の主役であるカルボカチオンやラジカルの運命を左右しているのです。この概念をマスターすれば、有機化学の世界がぐっとクリアに見えてくるはずです!

コメント