エタン、エチレン、アセチレンはそれぞれ酸性度が違って、
アセチレン>エチレン>エタン
の順番ですが、この理由を解説します。
目次
【理由】3つはそれぞれ違う混成軌道をとるから
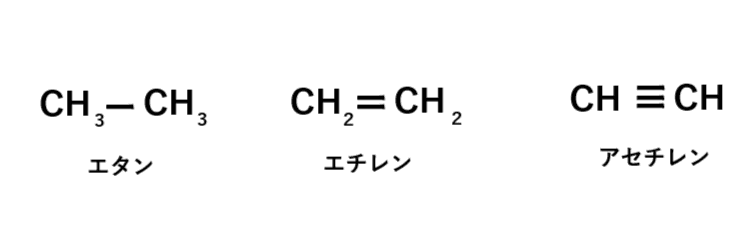
エタンはsp3混成、エチレンはsp2混成、アセチレンはsp混成ですよね。
つまり、s性の高さは「アセチレン>エチレン>エタン」という風になります。
(この理由ですが、例えばsp軌道のアセチレンは、s軌道とp軌道を一つずつ混ぜて、それを二つに分けてるのに対して、sp3軌道のエタンはs軌道1つとp軌道3つを混ぜて4分割してるので、一つ一つのs軌道の割合が低くなりますよね。)
s性が高いほど電子は原子核の近くにあるということになるので、その分負電荷を安定化させやすくなり、H+を放出しやすくなります。
というわけで、酸性度の強さはアセチレン>エチレン>エタンの順番だよってお話でした。

コメント
コメント一覧 (2件)
アセチレンの化学式は C2H2 なので構造式は CH三CH ではありませんか?
コメントありがとうございます!
その通りですね…申し訳ありません。
また何かあればコメントしてくださると嬉しいです!